化痔栓
本内容旨在为您提供一份关于中成药类别中化痔栓的详尽概览。化痔栓的药理分类为止血,ATC分类为治疗痔疮和肛裂的药物,目前化痔栓的国内上市企业有1家,包括广州白云山敬修堂药业股份有限公司、等。
此外,还有更多关于化痔栓的基本信息,如药品说明书、国内上市情况、国内药品临床试验登记...... 助您快速且全面地了解该药品。
- 药理分类: 理血剂/ 止血
- ATC分类: 心脑血管与血液系统药物/ 血管保护剂/ 治疗痔疮和肛裂的药物
- 剂型: —
- 医保类型: —
- 是否2018年版基药品种: 否
- OTC分类: —
- 中药保护品种: 否
- 是否289品种: 否
- 是否国家集采品种: ——
药品说明书
【说明书修订日期】
-
2015年11月02日
【警告】
-
本品含洋金花。
【药品名称】
-
通用名称: 化痔栓
汉语拼音:Huazhi Shuan
【成份】
【性状】
-
本品为暗黄褐色的栓剂。
【功能主治】
-
清热燥湿,收涩止血。用于大肠湿热所致的内外痔、混合痔疮。
【规格】
-
每粒重1.7克
【用法用量】
-
将药栓单个撕开(见图1),再从塑料片分离处撕开取出药栓(见图2),患者取侧卧位,置入肛门2~2.5厘米深处。一次1粒,一日1~2次。
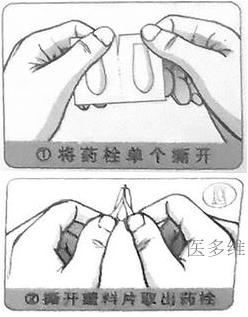
【不良反应】
-
尚不明确。
【禁忌】
-
尚不明确。
【注意事项】
-
1.本品为直肠给药,禁止内服。
2.忌烟酒及辛辣、油腻、刺激性食物。
3.保持大便通畅。
4.儿童、孕妇、哺乳期妇女及年老体弱者应在医师指导下使用。
5.有严重肝肾疾患及高血压、心脏病、糖尿病或血液病者应在医师指导下使用。
6.肛裂患者不宜使用。内痔出血过多或原因不明的便血,或内痔脱出不能自行还纳,均应去医院就诊。
7.药品宜存放在阴凉干燥处,防止受热变形。若因温度过高等原因致使药栓变软、熔化,但稍有变形、变软并不影响疗效,仍可将药栓冷冻后再撕开使用。
8.严格按用法用量使用,本品不宜长期使用。
9.用药3天症状无缓解,应去医院就诊。
10.对本品过敏者禁用,过敏体质者慎用。
11.本品性状发生改变时禁止使用。
12.儿童必须在成人监护下使用。
13.请将本品放在儿童不能接触的地方。
14.如正在使用其他药品,使用本品前请咨询医师或药师。
【药物相互作用】
-
如与其他药物同时使用可能会发生药物相互作用,详情请咨询医师或药师。
【特殊标记】
-
OTC甲类
外
【贮藏】
-
30℃以下密闭贮存。
【包装】
-
药用聚乙烯聚氯乙烯复合片材包装。每盒装2粒;每盒装5粒;每盒装10粒。
【有效期】
-
24个月
【执行标准】
-
《中国药典》2015年版一部。
【批准文号】
-
国药准字Z44022705
【生产企业】
-
企业名称:广州白云山敬修堂药业股份有限公司
生产地址:佛山市南海区黄岐鄱阳路249号
邮政编码:528248
电话号码:(028)81157723
传真号码:(020)81157740
注册地址:广州市荔湾区人民南路179号
邮政编码:510130
网 址:http://www.jxt.com.cn
如有问题可与生产企业联系
【修订/勘误1】
-
各省、自治区、直辖市食品药品监督管理局:
为保障公众用药安全,根据国家食品药品监督管理总局监测评价结果,现就含毒性中药饮片中成药说明书修订有关事项通知如下:
一、凡处方中含有《医疗用毒性药品管理办法》(国务院令第23号)中收载的28种毒性药材制成的中药饮片(含有毒性的炮制品)的中成药品种,相关药品生产企业应在其说明书【成份】项下标明该毒性中药饮片名称,并在相应位置增加警示语:“本品含XXX”。处方中含有其他已被证明具有毒性、易导致严重不良反应的中药饮片的中成药品种,相关药品生产企业也应按照上述要求修订说明书。
二、相关药品生产企业应主动跟踪药品临床应用安全性情况,根据不良反应监测数据及文献报道的相关安全性信息,按规定及时补充完善说明书【注意事项】等安全性内容。
三、涉及国家秘密技术的中成药品种应按照上述要求修订说明书。
四、相关药品生产企业应于2013年12月31日前,按上述要求,依据《药品注册管理办法》等有关规定提出修订说明书的补充申请报备案。说明书的其他内容应当与原批准内容一致。补充申请备案之日起生产的药品,不得继续使用原药品说明书。
五、相关药品生产企业应当将说明书修订的内容及时通知相关医疗机构、药品经营企业等单位,并在补充申请备案后6个月内对已出厂的说明书予以更换。
六、相关品种的标签涉及修订内容的,应当一并修订。国家食品药品监督管理总局办公厅
2013年11月4日
【修订/勘误2】
-
为保障公众用药安全,根据《处方药与非处方药分类管理办法(试行)》(国家药品监督管理局令第10号)的规定,经国家药品监督管理局组织论证和审定,将胃痛宁片、化痔栓及消栓通络制剂(片剂、胶囊剂、颗粒剂)调出非处方药目录,按处方药管理,同时对上述药品说明书进行修订。现将有关事项公告如下:
一、上述药品生产企业均应依据《药品注册管理办法》等有关规定,按照相关药品说明书修订要求(见附件1—3),提出修订说明书的补充申请,于2019年4月30日前报省级药监部门备案。
修订内容涉及药品标签的,应当一并进行修订;说明书及标签其他内容应当与原批准内容一致。在补充申请备案后6个月内对已出厂的药品说明书及标签予以更换。
上述药品生产企业应当对新增不良反应发生机制开展深入研究,采取有效措施做好相关药品使用和安全性问题的宣传培训,指导医师合理用药。
二、临床医师应当仔细阅读上述药品说明书的修订内容,在选择用药时,应当根据新修订说明书进行充分的效益/风险分析。
三、患者应严格遵医嘱用药,用药前应当仔细阅读相关药品说明书。
四、各省级药监部门应当督促行政区域内的上述药品生产企业按要求做好相应说明书修订和标签、说明书更换工作;对违法违规行为组织依法严厉查处。
特此公告。
附件:1.胃痛宁片说明书修订要求
2.化痔栓说明书修订要求
3.消栓通络制剂说明书修订要求国家药监局附件2:
2019年2月25日
化痔栓说明书修订要求
一、应注明“请仔细阅读说明书并在医师指导下使用”。
二、警示语应包括:
本品含洋金花。
三、【不良反应】项应包括:
1.皮肤及其附件:瘙痒、皮疹等。
2.消化系统:腹泻、腹痛等。
3.全身性反应:过敏样反应等。
4.精神神经系统:头晕等。
5.其他:心悸等。
四、【禁忌】项应包括:
1.儿童、孕妇、哺乳期妇女禁用。
2.高血压、心脏病、心动过速、青光眼患者禁用。
五、【注意事项】项应包括:
1.本品为直肠给药,禁止内服。
2.忌烟、酒及辛辣、油腻、刺激性食物。
3.保持大便通畅。
4.老年患者慎用。
5.有严重肝肾疾患及糖尿病或血液病患者慎用。
6.肛裂患者不宜使用。
7.本品含洋金花,应严格按用法用量使用,不宜过量或长期使用。用药后如出现说明书描述的不良反应或其他不适时应停药,症状严重者应及时去医院就诊。
8.药品宜存放在阴凉干燥处,防止受热变形。
9.对本品过敏者禁用,过敏体质者慎用。
说明书修订日期
警告
药品名称
成份
性状
功能主治
规格
用法用量
不良反应
禁忌
注意事项
药物相互作用
特殊标记
贮藏
包装
有效期
执行标准
批准文号
生产企业
修订/勘误1
修订/勘误2

查看更多药品说明书,请前往“合理用药”平台
国内上市情况
同成分全球上市情况
| 药品名称 | 公司名称 | 申请号/批准号 | 规格 | 剂型/给药途径 | 上市国家/地区 | 市场状态 | 日期 |
|---|---|---|---|---|---|---|---|
|
化痔栓
|
广州白云山敬修堂药业股份有限公司
|
国药准字Z44022705
|
1.4g;1.7g
|
栓剂
|
中国
|
在使用
|
2024-10-10
|

查看药品全球上市情况及详细数据,请前往“摩熵医药企业版”平台
药品中标情况
国内药品注册申报情况
国内药品临床试验登记
中药提取物备案
| 使用备案号 | 药品名称 | 生产企业 | 批准文号 | 备案状态 | 备案日期 | 中药提取物信息 |
|---|

查看更多中药提取物备案情况及详细数据,请前往“摩熵医药企业版”平台






