咪达唑仑口服溶液
本内容旨在为您提供一份关于西药类别中咪达唑仑口服溶液的详尽概览。咪达唑仑口服溶液的药理分类为镇静催眠药,ATC分类为苯并二氮卓衍生物类,目前咪达唑仑口服溶液的国内上市企业有1家,包括宜昌人福药业有限责任公司等。此外,还有更多关于咪达唑仑口服溶液的基本信息,如药品中标情况、同成分全球研发现状、国内药品临床试验登记...... 助您快速且全面地了解该药品。
- 药理分类: 治疗精神障碍药/ 镇静催眠药
- ATC分类: 精神安定药/ 催眠镇静药/ 苯并二氮卓衍生物类
- 剂型: —
- 医保类型: —
- 是否2018年版基药品种: ——
- OTC分类: ——
- 是否289品种: ——
- 是否国家集采品种: ——
药品说明书
【警告】
- 严禁用于食品和饲料加工 用于监测和复苏的设备和人员 咪达唑仑口服溶液可引起呼吸抑制和呼吸骤停,尤其是在非重症监护条件下使用时。也可引起呼吸衰竭、气道阻塞、血氧饱和度降低、缺氧和呼吸骤停,尤其是在与其他中枢神经系统(CNS)抑制剂联合使用时。 咪达唑仑口服溶液只能在能够提供呼吸和心脏功能连续监测的医院或门诊中使用(包括内科和牙科诊所)。确保能及时提供复苏药品以及与患儿年龄和体型相匹配的氧气袋/阀/而罩和气管插管设备。必须在经过培训能正确识别镇静深度,呼吸、循环抑制状态,能熟练进行各年龄段患儿的气道管理和心肺复苏的专业人员的观察与监护下给药。对于可能达到深度镇静的患儿,除了进行诊疗操作的医生外,还需专业人员全程监护,持续监测呼吸和心脏功能。 与阿片类药物联合使用的风险 苯二氮草类(包括咪达唑仑)和阿片类药物联用时,可导致深度镇静、呼吸抑制、昏迷和死亡。因此,当咪达唑仑和阿片类药物联用时,应监测患儿的呼吸抑制及镇静情况。
【药品名称】
-
通用名称:咪达唑仑口服溶液
商品名称:晓儿静
英文名称:Midazolam Oral Solution
汉语拼音:MiDaZuoLunKouFuRongYe
【成份】
-
本品主要成份为咪达唑仑。
化学名称:1-甲基-8-氯-6-(2-氟苯基)-4 H-咪唑并[1,5-a][1,4]苯并二氮杂䓬
化学结构式: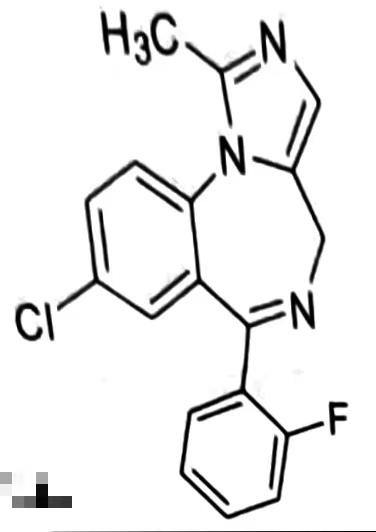
分子式:C18H13CIFN3
分子量:325.77
辅料:三氯蔗糖,山梨醇,依地酸二钠,盐酸和纯化水。
【适应症】
- 用于儿童诊断或治疗性操作前以及操作过程中的镇静/抗焦虑/遗忘;也可用于儿童术前镇静/抗焦虑/遗忘。
【规格】
- 0.2%(10ml:20mg)
【用法用量】
-
单次口服给药。推荐剂量为 0.25-0.5 mg/kg,最大剂量不超过 1.0 mg/kg,根据儿童患者(以下简称“患儿”)的年龄、焦虑程度、联合用药、操作配合度需求等个体化调整给药剂量,最大总给药剂量不超过 15 mg。
对镇静强度和镇静持续时间需求不强时,大龄患儿( ≥ 6 岁)或合作患儿建议采取较低剂量给药(0.25 mg/kg),不合作患儿可考虑较高剂量给药;对于患有心脏或呼吸系统疾病的患儿、其他高风险手术患儿、联合使用麻醉药或其他中枢神经系统抑制剂的患儿,建议采取较低剂量给药(0.25 mg/kg);低龄患儿( ≥ 6 个月,<6 岁)可能更易产生焦虑和恐惧感,母婴分离更困难,对镇静强度和镇静持续时间需求可能更大,所以低龄患儿可考虑采用较高剂量给药(0.5-1.0 mg/kg);肥胖患儿根据标准体重给药。
监测:
咪达唑仑口服溶液只能在能够提供呼吸和心脏功能连续监测的医院或门诊中使用(包括内科和牙科诊所)。确保能及时提供复苏药品以及与患儿年龄和体型相匹配的氧气袋/阀/面罩和气管插管设备。必须在经过培训能正确识别镇静深度,呼吸、循环抑制状态,能熟练进行各年龄段患儿的气道管理和心肺复苏的专业人员的观察与监护下给药。对于可能达到深度镇静的患儿,除了进行诊疗操作的医生外,还需专业人员全程监护患儿,持续监测呼吸和心脏功能。
患者对镇静药的反应及产生的呼吸状况是变化的,不管预期镇静程度及给药途径如何,镇静都是一个连续的过程。患者很容易从轻度镇静转成深度镇静,可能伴随保护性反射消失,特别是与麻醉药、其他中枢神经抑制剂和可能导致更强烈和持久镇静的药物联合使用时,患者出现呼吸抑制、气道阻塞或通气不足的风险增加,这种情况在儿童中尤为明显。使用咪达唑仑口服溶液的医生应了解并道循儿童镇静专业指南。与任何有潜在呼吸抑制的药物联用时,必须监测患儿心肺抑制状态。
镇静指南建议在给药前仔细了解患儿的病史以确定其基本医疗条件或合并用药情况是否可能影响患儿对镇静的反应,以及体检情况(尤其是呼吸道异常情况),并建议在给药前适当禁食。
尚未开展长期使用咪达唑仑口服溶液的研究。
【注意事项】
-
一般注意事项
咪达唑仑的有效性和安全性取决于给药剂量、患儿临床状态以及其他中枢神经抑制剂的合井用药情况。深度镇静时, 患儿可能会出现保护性反射消失, 特别是与麻醉药或其他中枢神经系统抑制剂合用时。必须根据患儿年龄、医疗/手术条件、联合用药等个体化调整咪达唑仑给药剂量, 且需准备与患儿体型相匹配的设备和设施以监测和干预患儿生命体征。使用咪达唑仑的医生必须具有处理合理、可预见的不良反应的能力,尤其是气道管理能力。
警告
1. 监测和复苏的人员与设备
咪达唑仑口服溶液只能在能够提供呼吸和心脏功能连续监测的医院或门诊中使用(包括内科和牙科诊所)。确保能及时提供复苏药品以及与患儿年龄和体型相匹配的氧气袋/阀/面罩和气管插管设备。必须在经过培训能正确识别镇静深度,呼吸、循环抑制状态,能熟练进行各年龄段患儿的气道管理和心肺复苏的专业人员的观察与监护下给药。对于可能达到深度镇静的患儿,除了进行诊疗操作的医生外,还需专业人员全程监护患儿,持续监测呼吸和心脏功能。应采用脉搏血氧仪等检测手段持续监测患儿以尽早发现如通气不足、气道阻塞或呼吸骤停的早期症状。若未及时治疗和处理通气不足、气道阻塞和呼吸骤停,可导致缺氧和/或心脏骤停。强烈建议马上使用特异性拮抗剂(氟马西尼)。恢复期也应持续监测生命体征。咪达唑仑可导致呼吸抑制,尤其是与阿片类激动剂和其他镇静药联合使用时,因此须在专业人员(能及时发现通气不足、进行气道管理和辅助吸氧)在场时,方可使用咪达唑仑用于镇静/抗焦虑/遗忘。
己有患儿术前口服咪达唑仑(麻醉诱导前镇静)后出现血氧饱和度下降、呼吸抑制、呼吸暂停和气道阻塞的报告。咪达唑仑与其他中枢神经系统抑制剂联用时,气道异常、紫绀型先天性心脏病、败血症或严重肺病患儿中发生上述不良反应的风险显著增高。
2. 与阿片类药物联合使用的风险
苯二氮草类(包括咪达唑仑)和阿片类药物联用时,可导致深度镇静、呼吸抑制、昏迷和死亡。因此,当咪达唑仑和阿片类药物联用时,应监测患儿的呼吸抑制及镇静情况。
3. 与呼吸系统不良事件相关的风险
口服咪达唑仑后可出现严重呼吸系统不良反应,包括呼吸抑制、气道阻塞、血氧饱和度下降、窒息、罕见呼吸和/或心脏骤停。尤其是咪达唑仑与其他中枢神经系统抑制剂联用时。单独口服推荐剂量咪达唑仑时,呼吸抑制、气道阻塞、血氧饱和度降低和呼吸骤停的发生率较低。
使用咪达唑仑前,需确保能及时提供复苏药品以及与患儿年龄和体型相匹配的氧气袋/阀/面罩和气管插管设备,具有经过培训能正确识别镇静深度,呼吸、循环抑制状态,能熟练进行各年龄段患儿的气道管理和心肺复苏的专业人员。
4. 剂量个体化
咪达唑仑口服溶液必须个体化给药,尤其是与其他中枢神经系统抑制剂联用时。(见用法用量)
5. 其他风险
有患儿和成人患者出现激动、无意识运动(包括强直/肌阵挛或痉挛及肌颤)、亢进、好斗等不良反应的报道,应将发生异常反应的可能性考虑在内。如果发生上述不良反应,在继续给药之前应综合评估咪达唑仑剂量、其他药物(包括局部麻醉药)的反应。有患儿和成人患者使用氟马西尼逆转上述反应的报道。咪达唑仑注射给药用于全身麻醉诱导,可观察到无眼疾患者眼压测量值中度降低。
6. 与中枢神经系统抑制剂联合使用
咪达唑仑与巴比妥类、酒精或其他中枢神经系统抑制剂联用可增加肺换气不足、气道阻塞、供氧不足、窒息发生的风险,同时会增加和/或延长药物的作用。麻醉术前用药也会抑制“由二氧化碳刺激引起的通气反应”。
7. 药物相互作用
服用酮康唑、依他康唑和沙奎那韦的患者体内咪达唑仑的血浆清除率降低,同时服用咪达唑仑口服溶液时会导致咪达唑仑的 Cmax和 AUC 大幅增加。因患儿有出现深度和持续镇静、呼吸抑制的风险,所以仅在必要时,方可联合使用咪达唑仑口服溶液和上述药物,且需配备专业的设备和人员,以处理呼吸功能不全。
8. 体弱和已有疾病患儿的注意事项
不管是否与其他镇静药合用,行高风险手术患儿需减少咪达唑仑剂量。心脏或呼吸系统受损的患儿对咪达唑仑引起的呼吸抑制更为敏感。行上呼吸道手术的患儿(如内窥镜、牙齿护理等),易因部分气道阻塞而发生血氧饱和度降低和通气不足。慢性肾功能衰竭和充血性心脏衰竭患儿对咪达唑仑的消除较慢。
9. 完整认知能力的恢复
注射咪达唑仑后,几小时内可出现记忆部分或完全遗忘。因此患儿注射咪达唑仑后(尤其是门诊患儿),应根据个体情况决定何时再从事需要集中精力的活动、操作危险机械等。用于评估咪达唑仑恢复情况的 Gross 测试,不能预测患儿承受压力时的反应时间。建议患儿在咪达唑仑的作用消退后如睡意消退,或者是麻醉和手术 24 h 后(以时间较长者计),才能操作危险机械,加强看护以确保人身安全。
10. 小儿神经毒性
已发表的动物试验表明,使用麻醉药和镇静药会阻断 NMDA 受体和/或增强 GABA 活性,从而发育中大脑的神经细胞凋亡增加,当使用麻醉药和镇静药超过 3 小时后会导致长期认知缺陷。上述发现的临床意义尚不清楚。基于现有数据,导致这些变化可能与妊娠晚期至出生后头几个月的暴露相关,但可能会延长到大约 3 岁。
一些已发表的儿童研究表明,在生命早期反复或长期接触麻醉药后可能会出现类似的缺陷,并可能导致认知或行为缺陷。这些研究具有很大的局限性,目前尚不清楚观察到的效果是麻醉/镇静药物还是其他因素(如手术或潜在疾病)导致的。
麻醉和镇静药物是儿童和孕妇医疗护理(需进行手术、或需其他择期手术或检查或需特定的安全药物)的重要部分,任何需要麻醉的择期手术的时间安排应考虑到该手术潜在风险和获益。
药物滥用和依赖
咪达唑仑口服溶液是一种苯二氮䓬类药物,为管制药品,依赖性与地西泮类药物相似。因此,咪达唑仑口服溶液可能会被滥用、误用、成瘾。苯二氮䓬类药物可导致身体依赖性,突然停药会导致患儿出现成断症状,长期服用咪达唑仑停药后出现的戒断症状与巴比妥类药物、酒精的戒断症状相似(抽搐、幻觉、震颤、腹部及肌肉痉挛、呕吐、出汗)。婴儿的主要戒断症状有:腹胀、恶心、吧吐、室性心动过速。
用药须知
为了保证安全有效地使用苯二氮䓬类药物,应向患儿/监护人告知以下信息和说明:
1. 患儿/监护人须告知医生是否饮酒、是否服用其他药物,特别是降压药、抗生素,包括非处方药。酒精能增强苯二氮䓬类药物的作用,因此,苯二氮䓬类药物治疗期间同时摄入酒精必须谨慎。
2. 医生应明确告知患儿/监护人咪达唑仑口服溶液的药理作用,例如镇静和遗忘,这些作用在某些患儿中可能会加重。口服咪达唑仑口服溶液后(尤其是门诊患儿),医生应根据个体情况决定何时再从事需要集中精力的活动、操作危险机械等。
3. 咪达唑仑口服溶液不应与葡萄柚汁同时服用。
4. 因为本品用药人群为患儿,因此服用后应严密看护以确保人身安全。
5. 麻醉药和镇静药物对大脑早期发育的影响:在动物幼崽和儿童中进行的研究表明,3 岁以下儿童反复或长期使用全身麻醉或镇静药物可能对其大脑的发育产生负面影响。需与父母和看护人讨论需要麻醉和镇静药物的手术或手术的获益、风险和手术持续时间。
【孕妇及哺乳妇女用药】
-
本品为儿童用药。
有关咪达唑仑的孕妇及哺乳期妇女用药信息如下:多个研究证实苯二氮䓬类药物(安定和利眠宁)使胎儿先天性畸形的风险增加,如果在怀孕期间使用咪达唑仑,必须告知咪达唑仑对婴儿的潜在威肋。咪达唑仑能透过胎盘屏障,孕妇在分娩前一周使用苯二氮䓬类药物对新生儿的中枢神经系统有抑制作用。咪达唑仑会随乳汁分泌。
【药理作用】
-
咪达唑仑是一种短效`的苯二氮䓬类中枢神经系统抑制剂。咪达唑仑具有催眠和镇静作用,其起效快、作用时间短。还具有抗焦虑、抗惊厥和肌肉松弛作用。咪达唑仑单次和/或多次给药^后,对精神运动功能有损伤,但是对血流动力学的影响极小。
苯二氦䓬类药物的中枢作用是通过增强抑制性突触的 GABA 能神经传递而介导的。当存在苯二氮䓬类药物时,通过正向变构调节增强了 GABA 受体对神经递质的亲和力,从而导致释放的 GABA 对突触后跨膜氯离子通量的作用增强。
【药理毒理】
-
遗传毒性
咪达唑仑 Ames 试`验、中国仓鼠肺细胞(V79)与人淋巴细胞染色体畸变试验、小鼠体内微核试验结果均为阴性。
生殖毒性
雄性大鼠自交配前 62 天开始经口给予咪达唑仑 1、4、16 mg/kg,雌性大鼠自交^配前 14 天至妊娠第 13 天或哺乳期第 21 天给予相同剂量的咪达唑仑。高剂量时暴露量(AUC)与人静脉注射咪达唑仑 4 mg/kg 的暴露量相当(根据体表面积折算,相当于人诱导剂量 0.35 mg/kg 的 1.85 倍),未见对雄性或雌性大鼠生育力的不良影响。
妊娠大鼠于器官发生期(妊娠第 7 至第 15 天)静脉注射给予咪达唑仑 0.2、1、4 mg/kg/天(按照体表面积折算,相当于人诱导剂量 0.35 mg/kg 的 0.09、0.46、1.85 倍),对大鼠胎仔未见不良影响;所有剂量均可导致轻度至中度的共济失调;高剂量使母体体重增重比对照组相比减少 5%。
妊娠兔于器官发生期(妊娠第 7 至第 18 天)静脉注射给予咪达唑仑 0.2、0.6、2 mg/kg/天(按照体表面积折算,相当于人诱导剂量 0.35 mg/kg 的 0.09、0.46、1.85 倍)对兔胎仔未见不良影响;高剂量可导致共济失调和镇静,但未见母体毒性。
大鼠于妊娠晚期至哺乳期(妊娠第 15 天至哺乳期第 21 天)静脉注射给予咪达唑仑 0.2、1、4 mg/kg/天(按照体表面积折算,相当于人诱导剂量 0.35 mg/kg 的 0.09、0.46、1.85 倍),所有剂量均引起共济失调;与对照组相比,高剂量使母体体重增重轻度降低;未见对子代有明显不良影响。该试验未对幼仔进行功能评估,如学习、记忆测试或生殖能力。
在一项已发表的灵长类动物试验中,在妊娠期第 122 天持续 24 小时给予麻醉制量的氯胺酮,可导致胎仔发育中大脑的神经元凋亡增加。在其他已发表的试验中,在妊娠第 120 天持续 5 小时给予异氟烷或异丙酚,导致子代发育中大脑的神经元和少突胶质细胞凋亡增加。就大脑发育而言,这个时间段对应于人类妊娠晚期。尚不清楚这些结果的临床意义:然而,幼龄动物试验表明神经细胞凋亡与长期认知缺陷有关。
致癌性
小鼠与大鼠连续 2 年掺食法给予马来酸咪达唑仑 1、9 和 80 mg/kg/天,高剂量组雌性小鼠可见肝脏肿瘤发生事明显增加。高剂量组雄性大鼠可见甲状腺滤泡细胞良性肿痛发生率轻度但有统计学意义的增加。马来酸咪达唑仑 9 mg/kg(按照体表面积折算,相当于人诱导剂量 0.35 mg/kg 的 4 倍)未见肿瘤发生率增加。尚不清楚这些种瘤的诱发机制。这些肿瘤是在动物长期给药后出现的,而人通常单次或数次用药。
依赖性
在用于评估精神药物的正向强化作用的灵长类动物模型中,咪达唑仑可使动物产生自身给药行为,食蟹猴使用咪达唑仑 5-10 周后,会产生轻至中度的驱体依赖性。
幼龄动物毒性
已发表的幼龄动物研究显示,在大脑快速生长期或突触发生期使用阻断 NMDA 受体或增强 GABA 活性的麻醉剂和镇静药物,如咪达唑仑注射,可导致发育中大脑的神经元和少突胶质细胞广泛丢失,以及突触形态和神经发生的改变。基于种属间的比较。这些变化的易损性窗口被认为与妊娠晚期至出生前几个月的暴露有关,但在人类中可能会延长至大约 3 岁。
在灵长类动物中,为产生轻度手术麻醉平面而暴露于氯胺酮 3 小时,未导致神经元细胞丢失增加,然而,给于异氟烷 5 小时或更长时间,神经元细胞丢失增加。啮齿类动物动物给予异氟烷和灵长类动物给予氯胺酮的数据提示,神经元和少突胶质细胞的丢失与学习和记忆方面的长期认知缺陷有关,尚不清楚这些非临床发现的临床意义,医护人员应权衡对孕妇、新生儿和年幼儿童适当麻醉的获益与这些非临床数据所提示的潜在风险。
【药代动力学】
-
吸/收
咪达唑仑经口服`后迅速吸收,肝肠首过消除作用显著。国外在不同年龄(6 个月到 16 岁)的患儿中对咪达唑仑和α-羟基咪达唑仑(咪达唑仑的主要代谢产物)的药代动力学、咪达唑仑口^服溶液的绝对生物利用度进行了研究,剂量范围为 0.25-1 mg/kg。这项研究的药代动力学参数如表 3 所示。不同剂量组(0.25、0.5 和 1 mg/kg)平均达峰时间为 0.17-2.65 h。6 个月到 16 岁的患儿口服 0.25-1 mg/kg(最大剂量为 40 mg)咪达唑仑后发现,咪达唑仑的药代动力学参数导线性变化。2 岁到 12 岁的患儿口服 0.25-1 mg/kg(三个剂量组,每组各有 18 例)咪达唑仑后发现,咪达唑仑的药代动力学参数呈线性变化。咪达唑仑口服溶液在患儿体内的绝对生物利用度约为 36%,与患儿年龄和体重无关。患儿口服咪达唑仑后,体内咪达唑仑和α-羟基咪达唑仑的 AUC 比值高于静注的(年龄为 6 个月到 16 岁,0.38-0.75 vs 0.21-0.39),患儿体内咪达唑仑和α-羟基咪达唑仑的 AUC 比值高于成人。
尚未研究食物对咪达唑仑口服溶液的影响。成人餐后口服 15 mg 咪达唑仑片剂,咪达唑仑的吸收不受影响。患儿镇静前一般禁食。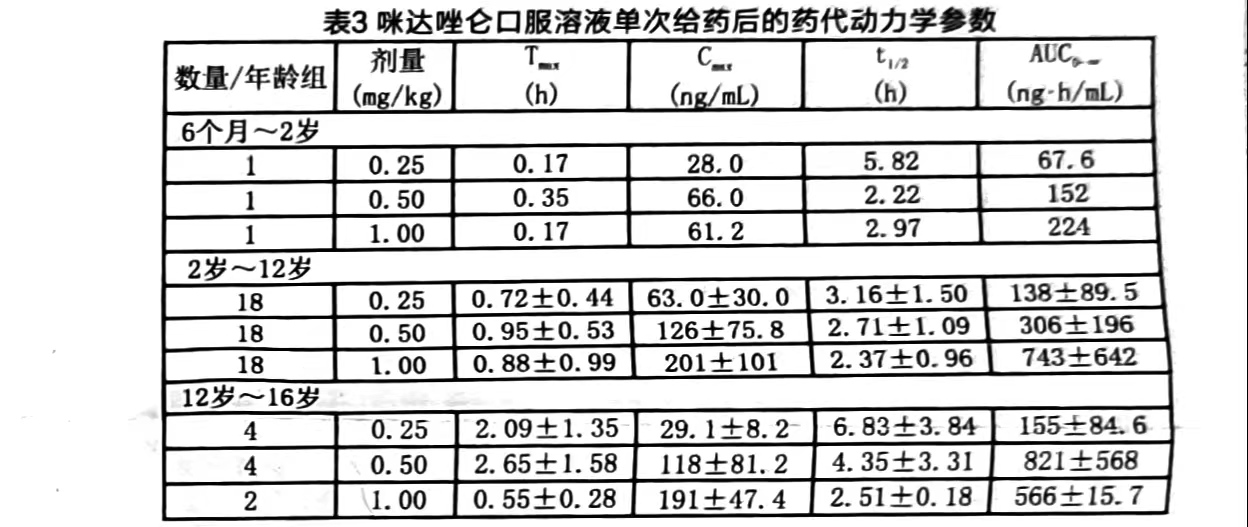
分布
咪达唑仑血浆蛋白结合率较高且与浓度无关。成人和 1 岁以上的患儿,咪达唑仑血浆蛋白结合率约 97%,主要与白蛋白结合。健康志愿者体内α-羟基咪达唑仑血浆蛋白结合率为 89%。患儿(6 个月-16 岁)静注 0.15 mg/kg 咪达唑仑后,平均稳态分布容积为 1.24-2.02L/kg。
代谢
咪达唑仑主要通过肝脏和肠道中的细胞色素 P4503A4(CYP3A4)代谢成活性代谢产物α-羟基咪达唑仑,在血浆中以葡萄糖醛酸结合物或非结合形式存在。最后主要以α-羟基咪达唑仑葡萄糖苷酸形式经尿液排泄。一项对成人志愿者静注咪达唑仑(0.1 mg/kg)或α-羟基咪达唑仑(0.15 mg/kg)的研究显示,两种化合物最大效应(Emax)和半数最大效应浓度(EC50)相似。研究影响因素有试验过程中的反应时间和试验误差。研究结果表明,在总体血浆浓度基础上,α-羟基咪达唑仑与咪达唑仑是等效的。口服或静脉注射给药后,63%-80% 的咪达唑仑以α-羟基咪达唑仑葡萄糖苷酸形式经尿排泄。在加入β-葡萄糖醛酸酶和硫酸酯酶前,尿中尚未检测出大量的原型药物或代谢产物,表明代谢产物多以结合物形式经尿液排泄。
咪达唑仑还有两种含量较少的代谢产物:4-羟基代谢物(大约占 3%)和二羟基代谢物(约为 1%),均以结合物形式经尿液排出。
消除
单次口服 0.25、0.5 和 1 mg/kg 的咪达唑仑(咪达唑仑口服溶液)后,其平均消除半衰期为 2.2-6.8 h。与患儿(6 个月到 16 岁)静注 0.15 mg/kg 咪达唑仑后的平均消除半衰期(2.9-4.5 h)相似。同一组患儿静脉注射 0.15 mg/kg 咪达唑仑后,其平均总清除率为 9.3-11.0 mL/min/kg。
【批准文号】
- 国药准字H20213321
【生产企业】
-
上市许可持有人:宜昌人福药业有限责任公司
注册地址:湖北省宜昌开发区大连路19号
企业名称:宜昌人福药业有限责任公司
生产地址:湖北省远安县鸣凤大道99号
电话号码:0717-6345005
邮箱:mail@ycrenfu.com.cn
网址:www.ycrenfu.com.cn
警告
药品名称
成份
适应症
规格
用法用量
禁忌
注意事项
孕妇及哺乳妇女用药
药理作用
药理毒理
药代动力学
批准文号
生产企业

查看更多药品说明书,请前往“合理用药”平台
国内上市情况
同成分全球上市情况
| 药品名称 | 公司名称 | 申请号/批准号 | 规格 | 剂型/给药途径 | 上市国家/地区 | 市场状态 | 日期 |
|---|---|---|---|---|---|---|---|
|
咪达唑仑口服溶液
|
宜昌人福药业有限责任公司
|
国药准字H20213321
|
0.2%(10ml:20mg)
|
口服溶液剂
|
中国
|
在使用
|
2021-04-27
|

查看药品全球上市情况及详细数据,请前往“摩熵医药企业版”平台
药品中标情况
- 最低中标价1.67
- 规格:15mg
- 时间:2014-12-16
- 省份:内蒙古
- 企业名称:江苏恩华药业股份有限公司
- 最高中标价0
- 规格:1ml:5mg
- 时间:2022-06-08
- 省份:陕西
- 企业名称:吉林四环澳康药业有限公司
| 药品名称 | 剂型 | 规格 | 转化系数 | 最小制剂单位价格(元) | 价格(元) | 生产企业 | 投标企业 | 省份 | 公布时间 | 网页链接 |
|---|---|---|---|---|---|---|---|---|---|---|
|
马来酸咪达唑仑片
|
片剂
|
15mg
|
10
|
3
|
30
|
江苏恩华药业股份有限公司
|
—
|
上海
|
2015-08-22
|
无 |
|
咪达唑仑注射液
|
注射剂
|
5ml:5mg
|
1
|
21.7
|
21.7
|
江苏恩华药业股份有限公司
|
西藏康健医药销售有限公司
|
西藏
|
2013-01-16
|
无 |
|
马来酸咪达唑仑片
|
片剂
|
15mg
|
10
|
1.81
|
18.1
|
江苏恩华药业股份有限公司
|
上海医药集团股份有限公司
|
上海
|
2011-04-26
|
无 |
|
咪达唑仑注射液
|
注射剂
|
2ml:2mg
|
1
|
5.38
|
5.38
|
江苏恩华药业股份有限公司
|
江苏恩华药业股份有限公司
|
宁夏
|
2010-12-26
|
无 |
|
马来酸咪达唑仑片
|
片剂
|
15mg
|
10
|
7.8
|
78
|
江苏恩华药业股份有限公司
|
江苏恩华药业股份有限公司
|
四川
|
2021-06-30
|
查看 |

查看更多药品招投标情况及详细数据,请前往“摩熵医药企业版”平台
国家集中采购情况
一致性评价
| 企业 | 品种 | 规格 | 剂型 | 过评情况 | 过评时间 | 注册分类 |
|---|---|---|---|---|---|---|
|
福安药业集团湖北人民制药有限公司
|
盐酸咪达唑仑口服溶液
|
10ml:20mg
|
口服液体剂
|
视同通过
|
2025-02-07
|
3类
|
|
江苏恩华药业股份有限公司
|
盐酸咪达唑仑口服溶液
|
118ml:236mg
|
口服液体剂
|
视同通过
|
2022-04-15
|
3类
|
|
福安药业集团湖北人民制药有限公司
|
盐酸咪达唑仑口服溶液
|
118ml:236mg
|
口服液体剂
|
视同通过
|
2025-02-07
|
3类
|
|
宜昌人福药业有限责任公司
|
咪达唑仑口服溶液
|
0.2%(10ml:20mg)
|
口服液体剂
|
视同通过
|
2021-04-29
|
3类
|
|
特丰制药有限公司
|
盐酸咪达唑仑口服溶液
|
10ml:20mg
|
口服液体剂
|
视同通过
|
2025-03-14
|
3类
|

查看更多过评企业情况及详细数据,请前往“摩熵医药企业版”平台
同成分全球研发现状
国内药品注册申报情况
| 受理号 | 药品名称 | CDE企业名称 | 申请类型 | 注册类型 | 承办日期 | 状态开始日期 | 办理状态 | 审评结论 |
|---|---|---|---|---|---|---|---|---|
|
CYHS2403647
|
咪达唑仑口服溶液
|
成都苑东生物制药股份有限公司
|
仿制
|
3
|
2024-10-26
|
—
|
—
|
— |
|
CXHL1400504军
|
咪达唑仑口服溶液
|
中国人民解放军军事医学科学院毒物药物研究所
|
新药
|
3.3
|
2014-06-16
|
2016-03-01
|
制证完毕-已发批件解放军总后卫生部 1009588027619
|
— |
|
CYHS2300610
|
咪达唑仑口服溶液
|
特丰制药有限公司
|
仿制
|
3
|
2023-02-22
|
—
|
—
|
查看 |
|
CXHL1400504
|
咪达唑仑口服溶液
|
中国人民解放军军事医学科学院毒物药物研究所
|
新药
|
3.3
|
2014-06-16
|
2016-03-01
|
制证完毕-已发批件解放军总后卫生部 1009588027619
|
查看 |
|
CXHL1200479
|
咪达唑仑口服溶液
|
宜昌人福药业有限责任公司
|
新药
|
3.1
|
2012-09-26
|
2015-10-28
|
制证完毕-已发批件湖北省 1054918447516
|
查看 |

查看更多药品审评情况及详细数据,请前往“摩熵医药企业版”平台
国内药品临床试验登记
| 登记号 | 试验专业题目 | 药物名称 | 适应症 | 试验状态 | 试验分期 | 申办单位 | 试验机构 | 首次公示日期 |
|---|---|---|---|---|---|---|---|---|
|
CTR20222101
|
评价磷酸安泰他韦胶囊/英强布韦片在健康受试者中对咪达唑仑口服溶液药代动力学影响的单中心、开放试验
|
咪达唑仑口服溶液
|
成人慢性丙型病毒性肝炎
|
已完成
|
Ⅰ期
|
广东东阳光药业有限公司
|
吉林大学第一医院
|
2022-08-19
|
|
CTR20231545
|
评价咪达唑仑口服溶液用于儿科人群医学检查、术前或治疗前镇静的有效性和安全性的单臂、多中心IV期临床研究
|
咪达唑仑口服溶液
|
用于儿童诊断或治疗性操作前以及操作过程中的镇静/抗焦虑/遗忘;也用于儿童术前镇静/抗焦虑/遗忘
|
已完成
|
Ⅳ期
|
宜昌人福药业有限责任公司
|
中南大学湘雅三医院
|
2023-05-24
|
|
CTR20201526
|
评价咪达唑仑口服溶液用于儿童医学检查前镇静的安全性、有效性和药代动力学特征的单臂临床试验。
|
咪达唑仑口服溶液
|
用于儿童在诊断、治疗、内窥镜检查前及麻醉诱导前镇静和抗焦虑。
|
已完成
|
Ⅲ期
|
新疆特丰药业股份有限公司、南京特丰药业股份有限公司
|
首都医科大学附属北京儿童医院
|
2020-08-03
|
|
CTR20170824
|
咪达唑仑口服溶液单中心、开放、随机、单剂量、两周期交叉人体生物等效性试验
|
咪达唑仑口服溶液
|
主要用于儿科患者诊断或治疗性操作、或内窥镜手术或麻醉诱导前的镇静、抗焦虑和顺行性遗忘。
|
已完成
|
BE试验
|
宜昌人福药业有限责任公司
|
华中科技大学同济医学院附属同济医院
|
2018-05-23
|

查看更多中国临床试验情况及详细数据,请前往“摩熵医药企业版”平台






